2022年6月2日
概要
京都大学医学部附属病院は、京都大学iPS細胞研究所(以下 CiRA)、公益財団法人京都大学iPS細胞研究財団(以下CiRA_F)および株式会社メガカリオン注1と連携し、ヒトiPS細胞由来HLAホモ型血小板(開発コード:MEG-002)の治験における、第一症例目の被験者への投与を問題なく完了したことをお知らせいたします。 ▶治験に関する詳細(京都大学医学部附属病院 血液内科 )
背景
京都大学医学部附属病院血液内科(髙折晃史教授)とCiRA(江藤浩之教授)のグループは、これまでに患者自身のiPS細胞由来血小板注2を使った臨床研究を実施してきました(CiRAニュース 2020年3月25日 )。 その後、単一の製剤で多人数に移植可能となるよう、あらかじめ健康なボランティアの方から作製したHLAホモ型の同種iPS細胞(iPS細胞ストック)由来血小板での企業治験の準備が完了していました(CiRAニュース 2021年4月26日 )。
経過
| 令和3年3月26日 | 治験計画届提出 |
| 令和3年4月26日 | 治験計画届30日調査終了 |
| 令和3年6月 7日 | 京都大学医学部附属病院 治験審査委員会に治験申請 |
| 令和3年6月21日 | 大学医学部附属病院 治験審査委員会承認 |
| 令和3年8月19日 | jRCT公開 |
| 令和4年4月 | 第一症例投与実施 |
第一例目 治験製品投与について
| 実施場所 | 京都大学医学部附属病院 |
| 投与時期 | 令和4年4月 |
| 治験調整医師 | 血液内科 髙折 晃史 教授 |
| 治験責任医師 | 血液内科 諫田 淳也 講師 |
| 治験製品 | MEG-002(ヒトiPS細胞由来血小板製剤) |
| 用量 | 3単位(血小板0.6x1011個) |
| 製造場所 | CiRA_F 細胞調製施設FiT |
治験概要
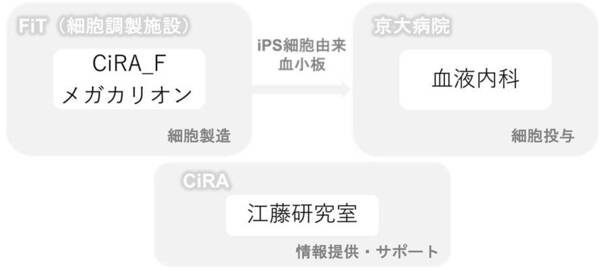
本治験では、血小板減少症注3の患者を対象に、「MEG-002」の安全性の確認と有効性の推定を行います。 「MEG-002」は、CiRAより提供を受けたiPS細胞から作製された、日本人において最も発現頻度が高いHLA型を有する血小板であり、 開発にあたっては同研究所の江藤浩之教授等が発明したヒトiPS細胞から血小板を産生する技術を用いています。なお治験製品の製造はCiRA_Fが担い (CiRA_Fニュース2020年6月22日 )、 治験は京都大学医学部附属病院血液内科をはじめとした複数の医療機関で実施を予定しています。
治験の名称
血小板減少症患者を対象としたiPS細胞由来血小板製剤(MEG-002)の忍容性及び安全性並びに有効性に関する探索的臨床試験 詳細情報:jRCT公開ページ JRCT番号:jRCT2053210068
治験の目的
血小板減少症におけるMEG-002単回投与時の忍容性、安全性および有効性の評価を目的とする
治験のデザイン
第1/2相試験 非盲検非対照試験/単回投与試験
主要評価項目
安全性(有害事象、副作用の発現割合)有効性(補正血小板増加数注4))
治験対象者
(1)以下の疾患などに基づく血小板減少症で、病状が安定している患者
本治験への支援
ヒトiPS細胞由来HLAホモ型血小板の実用化については、下記機関より支援を受けました。 ・国立研究開発法人日本医療研究開発機構(AMED) 「医療研究開発革新基盤創成事業(CiCLE)」 研究開発課題名: iPS細胞由来HLAホモ型血小板の実用化
用語説明
注1 株式会社メガカリオン
本社:京都府京都市下京区、代表取締役社長:赤松 健一
URL:http://www.megakaryon.com/
CiRA江藤浩之教授等の発明によるヒト iPS 細胞から血小板を産生する技術の臨床応用を目指して2011年に設立。ヒト iPS 細胞由来血小板製剤を工業的に大量生産することによって、世界の医療現場へヒト iPS 細胞由来血小板製剤を供給することを目指している。
注2 ヒトiPS細胞由来血小板
ヒトiPS細胞から分化させた巨核球前駆細胞に3つの遺伝子を導入することで得られる凍結保存可能な不死化巨核球細胞をマスターセルバンク化し、このマスターセルバンクから培養した巨核球を成熟させることによって血小板を産生します。
注3 血小板および血小板減少症について
血小板は血液中の細胞成分のひとつであり、巨核球と呼ばれる細胞から作られ、全身を循環し、血管壁が損傷した際に傷口に集まって止血する役割を持っています。血小板減少症とは血中の血小板数が少ない状態をいい、血小板数が一定数以下となった場合や出血の危険性が高いと認められる場合には、輸血用血小板製剤での治療が行われます。
注4 補正血小板増加数
体格(体表面積)で補正した輸血で増加した血小板数の値。血小板輸血の効果の指標として用いられます。